バイオ医薬品企業の経営者が取るべき戦略的行動
イノベーションを推進する上で、大手と中小の製薬企業は異なる役割を果たしながらも、相乗的な効果を担っています。中小企業は斬新なアイデアを生み出し、大手企業はそれらのアイデアを市場をリードする治療法に変えることができる規模とリソースを提供できます。バイオ医薬品のエコシステム全体にわたり、新たな機会を解き放ち、より大きな価値を推進するために、大手と中小が担うこれらの相互効果を発展させていく必要があります。
大手製薬企業の経営者は、R&D生産性を具体的に次のように移行させる必要があります。
- 収益の成長につながる超ブロックバスターとなる特異なアセットを作り出すために、目標を十分に達成できるポートフォリオを構築する。そのために、ポートフォリオの優先付けに関するより厳しい基準を保つ。
- 初期段階の科学研究へのアクセス、臨床開発 におけるスピード、治療法の適用範囲の拡大、および開発の成功率を最適化することにより、社内のイノベーション創出に投資する。大手製薬企業が前臨床の段階において発見または買収した新薬候補は、開発の後期段階において取引コストを掛けて外部から取得した場合よりも、平均的に高い収益を生み出します。
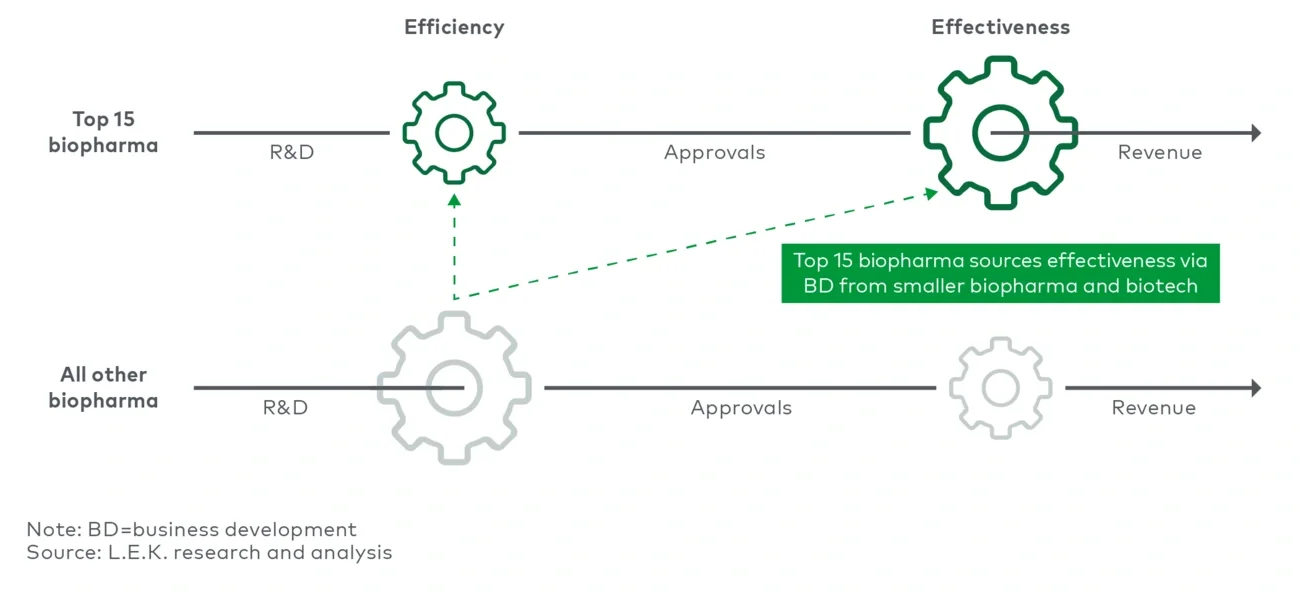
- より選別された案件に絞って事業開発を行う。大手製薬企業において、事業開発は非常に重 要な活動であることに変わりはありません。しかしながら、R&D生産性を向上させる上で高いコストが掛かる可能性があります。そのため、大手製薬企業は、R&D生産性に対する事業開発活動の貢献度を慎重に考慮し、状況に応じてこれまでとは異なるアプローチをとる必要があります。
また、中小企業の経営者は、次のことに集中的に取り組む必要があります。
- R&D効率性の維持と向上。これまで中小企業は、少数チーム、限られた資本、効率性重視により優れた成果を収めてきました。しかし、成長するにつれ、高価値な資金調達によりさらに大きな資本プールへのアクセスが可能になると、この重要な要素を失う恐れがあります。R&Dの効率性を維持するためには、初期段階のプログラムにおいて機動性と財務規律を重視し、最小限のリソースの消費で最大限の効果が得られるよう適切に設計された実験や臨床試験を優先していく必要があります。適応性と規律を保つことで、革新的で機敏性のある文化を犠牲にすることなく規模の拡大を図ることができます。
- リードアセットの臨床開発の再検討。中小企 業は、初期の臨床 PoC(Proof of Concept)を確保するために、ニッチな治療法に対してリードアセットの開発を集中させる傾向があります。多くの場合、このアプローチをとる背景には財政的制約がありますが、長期的には将来性に制限を加えてしまう可能性があります。これらの企業の経営者は、可能な限り、規模が大きく価値の高い治療法をターゲットとした野心的な戦略を検討していく必要があります。達成するためには資金調達や提携における工夫が必要になりますが、これらの分野を積極的に探索することは、より高い企業価値と株主価値をもたらすことにつながります。
- 価値を維持するための取引の検討。バイオテクノロジーのプラットフォームは、予想していなかった治療への適用が判明することがしばしばあります。そのため、単独で参入できる小規模範囲を対象とした治療法と、大手製薬企業との提携を通じた規模の大きい競争市場を対象とした治療法との間での戦略的なバランスが必要となります。資産価値を最大限に引き出すために提携が必要である場合、早い段階で価値を過度に 手放してはいけません。共同開発や共同販売契約、有利なマイルストーンペイメントなどを通じて、長期的なメリットを確保できるよう取引をまとめる必要があります。
これらの戦略を優先的に実行することで、バイオテクノロジーと製薬業界の経営者は、イノベーションと規律を重視したプロセスを通じて、進化と競争の激しいバイオ医薬品のエコシステムの中で効果的なかじ取りを行うことができます。その結果、R&D生産性を高め、継続的な成功を収めることにつながります。
本稿に対してご協力をいただいたL.E.K.ヘルスケ ア・インサイト・センターのジェニー・マッキー氏とイーサン・ヘルベリ氏に著者から感謝の意を表します。
詳細については、こちらまでお問い合わせください。
L.E.K.Consultingは、L.E.K. Consulting LLC.の登録商標です。この文書に記載されているその他すべての製品およびブランドの所有権は、各所有者にあります。 © 2025 L.E.K.Consulting LLC
巻末注
1バイオ医薬品企業上位15社は、2024年のバイオ医薬品による収益が250億
ドルを超える企業をもとに分類(Evaluate Pharmaによる推定値)。上位15社以外の企業は、その他の革新的なバイオ医薬品とバイオテクノロジー企業として定義(ジェネリック医薬品、機器、サービス、プラットフォーム、テクノロジーを扱う企業を除く)。
2Genengnews.com, “The Great Pharma Wasteland”, https://www. genengnews.com/topics/drug-discovery/the-great-pharma- wasteland/
3Nature.com、「イールームの法則を破る」、https://www.nature.com/
articles/d41573-020-00059-3